Теории старения
| д.м.н., профессор Потехина Ю.П.
Современная наука знает слишком мало В литературе можно встретить множество определений старения, но смысл у них примерно одинаковый. Старение - неизбежно возникающий, закономерно развивающийся разрушительный процесс адаптационных возможностей организма, увеличения вероятности смерти, сокращения продолжительности жизни, способствующий развитию возрастной патологии. Для развития старения характерно:
 Основными чертами процесса старения являются:
 Старение может быть физиологическим и патологическим. Преждевременное старение может быть обусловлено следующими факторами:
1.Отсутствие универсального набора тестов для определения биологического возраста, который был бы более надежен, чем хронологический возраст. 2.Большинство измеряемых показателей изменяется с возрастом постепенно, а не скачкообразно. 3.Скачкообразные изменения более свойственны развитию ассоциированной с возрастом патологии. 4.Возрастные изменения: а) не являющиеся патологией (поседение волос) б) изменения, которые могут способствовать развитию патологических процессов (накопление оксидативных изменений) В 1903 году И.И.Мечников предложил термин «геронтология» (от греч. gerontos - старик и logos - учение). Геронтология - это наука о причинах, механизмах и закономерностях старения, об изменениях в стареющем организме, о влиянии этих изменений на жизнедеятельность и продолжительность жизни, о мерах по ее продлению. Теории старения. Теории старения должны отвечать на следующие вопросы:
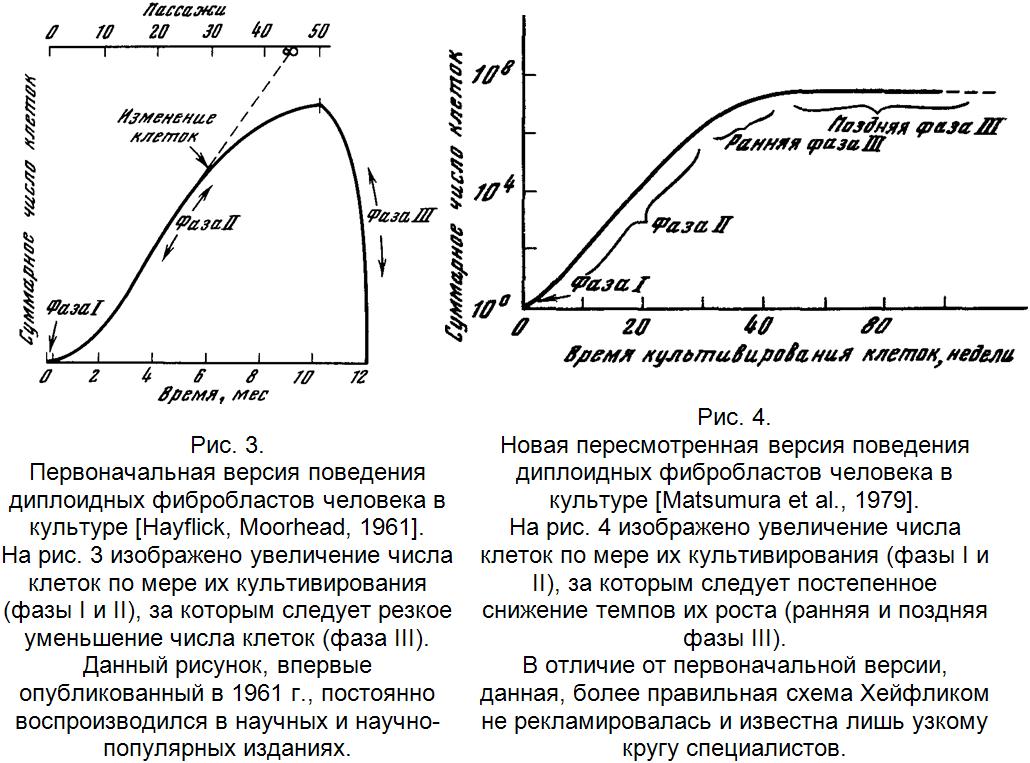
К сегодняшнему дню так и не создано единой теории старения. Существует несколько десятков теорий старения, и это само по себе говорит об отсутствии общепринятой концепции. Почти все они сводятся к вариациям двух тем: 1) старение - это процесс генетически запрограммированный; 2) старение - это стохастический, случайный процесс , обусловленный "изнашиванием" организма в результате самоотравления продуктами жизнедеятельности и/или повреждения, наносимого постоянно действующими вредными факторами среды. А.Вейсман (1884) одним из первых обратился к эволюционной аргументации в обосновании величины и механизмов продолжительности жизни и процесса старения. Естественная смерть организма, обеспечивая выгодную для вида смену поколений, появляется как адаптивный признак вследствие отбора, направленного на сокращение длительности жизни особи. Все варианты "генетических" теорий старения проистекают из концепции Вейсмана, который предположил, что максимальная продолжительность жизни детерминирована генетически в виде числа поколений соматических клеток многоклеточного организма. Казалось бы, современная наука доказала гипотезу Вейсмана об ограничении продолжительности жизни организма за счет заложенных в геноме "часов". Так, фибробласты (клетки соединительной ткани), изъятые из организма и помещенные в полноценную среду, способны лишь к ограниченному числу делений около 50 (число Хейфлика), после чего культура гибнет [Hayflick, 1974]. Недавно стал известен молекулярный механизм, ограничивающий число делений фибробластов в культуре - снижение в стареющих культурах активности теломеразы - одного из ферментов, обеспечивающих сохранение свойств ДНК в последовательных поколениях клеток. Многочисленные публикации Хейфлика 60-х и 70-х годов были восприняты многими как научная сенсация, открывающая принципиально новый подход к выяснению механизмов детерминации продолжительности жизни. В 1978 г российским ученым Л.А.Гавриловым была проведена ревизия концепции Вейсмана-Хейфлика, в результате которой были сделаны следующие основные выводы:
Нетрудно заметить, что с учетом новых фактов феномен Хейфлика уже не столь очевидным образом связан с проблемой ограниченной продолжительности жизни организмов. Действительно, массовая гибель клеток могла бы приводить к гибели организма, в то время как из снижения темпов роста клеточной популяции ограниченность сроков жизни организма прямо не следует. Более того, снижение митотической активности является нормальным физиологическим процессом, связанным с дифференцировкой клеток. Выполнение высокоспециализированной функции оказывается несовместимым с клеточным делением (нервные и мышечные клетки). Вместе с тем, очевидно, что переход части клеток в постмитотическое состояние создает предпосылки к снижению регенераторных возможностей организма и в конечном итоге к уменьшению числа функционирующих клеток, что действительно наблюдается с возрастом. Поэтому исследование кинетики клеточных популяций на разных этапах жизни организма может иметь важное значение для выяснения механизмов, определяющих продолжительность жизни. Теломеры являются структурами на концах линейных хромосом, состоящими из гексануклотидных (TTAGGG) повторов. В отсутствие компенсаторного механизма у делящихся клеток происходит постепенное разрушение теломеров до критической степени сокращения, что приводит к хромосомным аномалиям и клеточной смерти или старению. Экспрессия теломеразы - фермента, удлиняющего теломеры, подавляется рано в развитии во всех нормальных человеческих соматических тканях, в то время как активность и экспрессия РНК компонента этого энзима происходит почти во всех случаях злокачественной трансформации и рака поздней стадии. Теломерная гипотеза старения постулирует, что достаточная потеря теломеров на одной или нескольких хромосомах в нормальных соматических клетках способствует клеточному старению. Поскольку теломеры в большинстве человеческих клеток сокращаются в процессе старения, то длина теломеров может быть биомаркером старения и связанной со старением заболеваемости Клетки долгоживущих видов способны совершить больше делений (А.М.Оловников). Оказалось, что эмбриональные фибробласты мыши способны удвоить свою численность in vitro всего 14-28 раз, цыпленка - 15-35, человека - 40-60, а черепахи - 72-114 раз. В течение последних лет ведется интенсивный поиск кандидатов на роль генов старения и долголетия у человека. Шахтер и соавт. предложили классификацию таких генов:
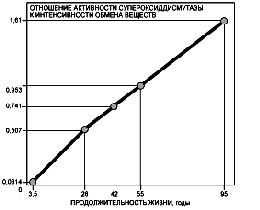
Ген bcl-2 блокирует апоптоз, что продлевает жизнь клеток. Продукт гена bcl-2 препятствует токсичному эффекту гидроксильных радикалов, защищая стареющие клетки от окислительного стресса. Ген белка р53 выполняет функцию удаления старых нефункционирующих клеток. Гены аполипопротеина Е (АпоЕ) н ангиотензинпревращающего фермента играют важную роль в липидном метаболизме и непосредственно влияют на продолжительность жизни. Внутри гена, ответственного за синдром Вернера (синдром преждевременного старения), были обнаружены особые участки ДНК, называемые Alu-последовательности. Подобные участки раньше считали "балластной" ДНК, служащей чем-то вроде прослойки между генами, несущими информацию о белках. Сегодня стало ясно, что Alu-последовательности играют какую-то особую роль, связанную, возможно, с регуляторными функциями генов. Они чаще, чем другие участки ДНК, подвергаются изменениям, мутациям. Полигенная система главного комплекта гистосовместимости (HLA) может играть важную роль среди генетических факторов долгожительства. У столетних, по сравнению с более молодыми возрастными группами, в 2 раза чаще встречаются некоторые аллели HLA-A, HLA-C и DR. Роль специфичных хромосом в старении. Гены, определяющие старение, не распределены случайно по всем хромосомам. В настоящее время проводится интенсивная работа по идентификации таких генов и определению мест их локализации. При кариотипическом анализе бессмертных клонов гибридов нормальных человеческих диплоидных фибробластов установлено, что обе копии 1-й хромосомы утеряны. Введение хотя бы одной копии 1-й хромосомы в клетку методом внутриклеточной инфузии вызывало типичную картину клеточного старения, что не было обнаружено ни для одной другой хромосомы. Мутация гена, расположенного в 9-ой хромосоме, приводит к синдрому ускоренного старения (в нем были обнаружены Alu-последовательности, которые чаще других подвергаются мутациям). Геронтологи, рассматривающие проблему старения и долгожительства как комплексную, скептично относятся к перспективе решить ее за счет замены "плохих" генов на "хорошие". По их мнению, вклад наследственных факторов в среднюю продолжительность жизни не превышает 25%. Роль ненаследственных факторов акцентируется в группе теорий старения за счет изнашивания организма. В ходе жизнедеятельности в нем накапливаются токсические продукты обмена веществ, он постоянно подвержен действию вредных внешних факторов [Комфорт А., 1967]. Обезвреживающие механизмы, которые у молодых организмов еще устраняют повреждения, постепенно изнашиваются, и одряхление становится все более явным. Так, согласно свободно-радикальной теории старения [Harman D., 1956], в результате неких "ошибок метаболизма" в цитоплазме появляются в большом количестве свободные радикалы (атомы или молекулы, имеющие неспаренный электрон на внешней орбитали), в частности, разнообразные "активные формы кислорода" - АФК (супероксид-анион радикал, продукты распада перекиси водорода и реакций с ее участием, окислы азота и т. д.). Пpодуциpуемые главным образом в митохондриях, АФК вызывают повpеждения мембpан, коллагена, ДНК, хpоматина, стpуктуpных белков, а также участвуют в эпигенетической pегуляции экспрессии ядерных и митохондриальных генов, приводя к метилированию ДНК, влияют на внутpиклеточный уpовень кальция, запускают каскад, ведущий к апоптозу и т.д. Утверждается, что с возрастом свободные радикалы обезвреживаются антиоксидантной системой все хуже и все активнее нарушают работу "молекулярных машин" клетки. На сегодняшний день достаточно убедительно доказано участие активных форм кислорода в механизмах формирования заболеваний, часто встречающихся у лиц пожилого и старческого возраста, таких как атеросклероз и злокачественные новообразования. С возрастом безусловно повышается содержание в тканях человека и животных продуктов окислительного повреждения макромолекул, в том числе ДНК. Наиболее значимым при старении оказывается усиленное перекисное окисление белков, чему способствует снижение активности СОД как результата снижения общей продукции АФК (АнисимовВ.Н., 1999). Повреждение под действием АФК макромолекул приводит к мутациям, нестабильности генома в целом и развитию ряда возрастных патологий: рак, сердечно-сосудистые заболевания, возрастная иммунодепрессия, дисфункция мозга, катаракта и др. Американский геронтолог Р.Катлер показал, что продолжительность жизни животных и человека определяется соотношением активности супероксиддисмутазы (одного из основных ферментов-антиоксидантов) к интенсивности обмена веществ (Рис. 5).
 Старение это процесс, реализующий смертность, то есть временную дискретность организмов, необходимую для смены поколений. Без этого виды не могут сколь-либо длительно приспосабливаться к изменениям окружающей среды. Старение универсально, что обосновывает необходимость поиска общего для всех эукариот механизма действия этого процесса.
В исследовании стохастических механизмов старения важное значение может иметь многолетний опыт эксплуатации сложных технических систем, поскольку он позволяет выявить основные параметры, существенные для обеспечения работоспособности (жизнеспособности) изучаемых объектов: 1. Устойчивость - важнейшая характеристика системы, состоящая в способности автоматически восстанавливать свое состояние после внезапного нарушения последнего каким-нибудь внешним или внутренним фактором. С возрастом организма происходит значительное падение динамической устойчивости по отношению к целому ряду возмущающих факторов, например, уменьшение толерантности к глюкозе. 2. Точность выполнения операций - качество приближения ее практического выполнения к (теоретическому) заданному способу. Отклонение от этого идеального способа характеризует величину ошибки. Имеются данные о снижении точности выполнения операций с возрастом организма. ДНК-полимераза, выделенная из старых организмов, гораздо чаще ошибается, включая в ДНК некомплементарные нуклеотиды [Holliday, Kirkwood, 1981]. Другим примером является снижение способности Т-лимфоцитов распознавать собственные белки-антигены, что приводит к росту аутоиммунных заболеваний в старости [Walfbrd, 1983]. У старых мышей частота ошибок при прохождении лабиринта достоверно выше, чем у молодых, несмотря на предварительную тренировку и отбор только хорошо обученных особей [Ingram et al„ 1987]. 3. Быстродействие - среднестатистическое число операций, выполняемых в единицу времени. С возрастом организма быстродействие многих его систем снижается, например, уменьшается скорость распространения нервного импульса [Стрелер, 1964, Walfbrd, 1983]. 4. Нагрузочная характеристика - параметр, характеризующий связь между величиной нагрузки и ответом системы. При старении снижается диапазон изменения ответа системы на стимул. В ответ на действие гормона ткани старого организма начинают реагировать при меньших его концентрациях, но величина максимального ответа при высоких концентрациях гормона у них понижена. В 1978 г Л.А.Гавриловым была выдвинута гипотеза о том, что старение организмов обусловлено "каскадом зависимых отказов", возникающим в результате случайного отказа одной из систем организма. Выход значений вышеперечисленных параметров за допустимые пределы в теории надежности называют отказом. Различают внезапные отказы, когда происходит скачкообразное изменение одного или нескольких основных параметров устройства (например, гибель клетки), и постепенные отказы, которые соответствуют медленному изменению значений одного или нескольких параметров устройства (например, атрофия клетки). Кроме того, отказы делят на независимые и зависимые Независимые отказы соответствуют отказу элемента устройства, не обусловленного повреждением других элементов (травма). Зависимый отказ - это отказ, возникший в результате повреждения или выхода из строя других элементов. Поскольку в биологических системах существование одних органов полностью зависит от нормального функционирования других, зависимые отказы имеют очень большое значение. Достаточно даже небольшого восстанавливаемого отказа в одной из систем организма (например, образования тромба в коронарном сосуде), чтобы вызвать целый каскад зависимых и невосстанавливаемых отказов всех остальных систем. Поэтому большинство систем организма является избыточным по числу функционирующих элементов. Такое резервирование обеспечивает нормальную работу системы в целом даже при временном отказе большой группы элементов Однако уменьшение числа элементов с возрастом (снижение кратности резервирования) ведет к резкому снижению надежности системы и увеличению вероятности смерти. В качестве примера можно привести процесс развитие некомпенсированного сахарного диабета: относительная инсулиновая недостаточность ? длительная гипергликемия ? полное истощению инсулинпродуцирующей способности островкового аппарата поджелудочной железы ? переход относительной инсулиновой недостаточности в абсолютную ? почечная недостаточность и поражение сердечно-сосудистой системы ? развитие нефрогенной гипертензии, которая может закончиться смертью от инсульта. В.Дильман (1952) считает, что у высших организмов, включая человека, старение непосредственно связано с механизмом развития, а именно те же самые факторы, которые обеспечивают развитие организма, продолжают действовать и после его завершения, являясь одновременно и причиной, приводящей к старению. Естественная смерть - смерть регуляторная. Если жизнь возможна только при соблюдении стабильности внутренней среды, то развитие и рост не могут осуществляться без нарушения закона стабильности. Фундаментальный закон постоянства внутренней среды может существовать только в диалектическом единстве со своей противоположностью - законом отклонения гомеостаза . Для того чтобы оба противоположных закона могли сосуществовать, обеспечивая стабильность в каждый данный момент и развитие во времени, необходимо, чтобы оба закона выполнялись по аналогичным правилам, что обеспечивается регуляторными системами организма во главе с гипоталамусом. Развивая и углубляя на протяжении почти 40 лет свою концепцию, В.М. Дильман пришёл к убеждению, что старение (и главные болезни, сцепленные со старением) не запрограммировано, а есть побочный продукт реализации генетической программы развития и поэтому старение возникает с закономерностью, свойственной генетической программе. Из онтогенетической модели возникновения болезней следует, что их развитие можно затормозить, если стабилизировать состояние гомеостаза на уровне, достигаемом к окончанию развития организма. «Нормальные» болезни старения: Одной из наиболее частых причин инвалидности и смерти у пожилых людей являются злокачественные новообразования. Есть несколько гипотез, объясняющих связь процессов старения и канцерогенеза: Более 30 лет назад В.В.Фролькис выдвинули адаптационно-регуляторную теорию возрастного развития. Адаптационной она называется потому, что объясняет главное: почему развивается старение, почему при старении сокращаются приспособительные возможности организма - основа снижения качества жизни, развития болезней, увеличения вероятности смерти. Регуляторной она называется потому, что объясняет наступающие с возрастом изменения нарушениями саморегуляции. В организме все регулируется, однако, в возрастных изменениях особое значение имеют сдвиги на двух уровнях: Именно на этом пути анализа фундаментальных механизмов старения группе сотрудников Института геронтологии АМН Украины удалось доказать, что наряду с процессом старения существует и процесс антистарения или витаукт (от лат. vita - жизнь, auctum - увеличивать). Антистарение потому и является витауктом, что не только противодействует старению, но и приводит к новым формам функциональной организации, способствующим увеличению адаптационных возможностей организма в эволюции. Проявление процесса антистарения удалось выявить на разных уровнях жизнедеятельности организма. К примеру, система "репарации" генетического аппарата; система обезвреживания свободных радикалов, гипертрофия и многоядерность клеток и др. Одни механизмы антистарения направлены на создание более надежных, менее разрушаемых, менее подверженных старению систем; другие на компенсацию, ликвидацию последствий старения. Баланс процессов старения и антистарения определяет продолжительность жизни, долговечность организма.
Старение может быть последствием хронического стресса. Способность восстанавливаться после стресса с возрастом снижается. В генетически гетерогенных популяциях человека динамика способности поддерживать адекватную реакцию на стресс сходна с зависимостью выживаемости от возраста (De Benedictis, 2001). Литература: |